Важка вода

Ми звикли, що формула води H2O означає, що вона містить два атоми водню та один атом кисню. У типовому стані атом водню має заряд 1, тобто в його ядрі знаходиться один протон, його називають протієм. Але існують і особливі атоми, які містять два (дейтерій) або три (тритій) протона в ядрі. Вони називаються ізотопами. Їхні хімічні властивості настільки близькі до атомів звичайного водню, що вони з легкістю утворюють такі ж молекули.
Відповідно, можуть існувати кілька модифікацій звичної нам води.
Склад і властивості важкої води
Найбільш поширеною є протіева або звичайна вода (H2O). Вона становить близько 99,985% загальної маси води на планеті. Решта 0,015% можуть складатися з молекул, які містять різні ізотопи водню згадані вище, а також кисню.
Найпоширенішою модифікацією є напівважка вода (HDO), яка містить один атом звичайного водню (протію) і один атом дейтерію, вона становить основну масу важкої води в цілому. Але фактично завдяки реакціям ізотопного обміну, вона являє собою суміш H2O, HDO, D2O в приблизному співвідношенні 2: 1: 1.
Надважку воду в складі містить тритій. Загалом до неї належить 9 модифікацій, тобто існує 9 формул важкої води, які містять в різних співвідношеннях протій, дейтерій, тритій і ізотопні модифікації кисню - 16O, 17O, 18O та ін. Вміст надважкої води критично малий — до декількох молекул в літрі.
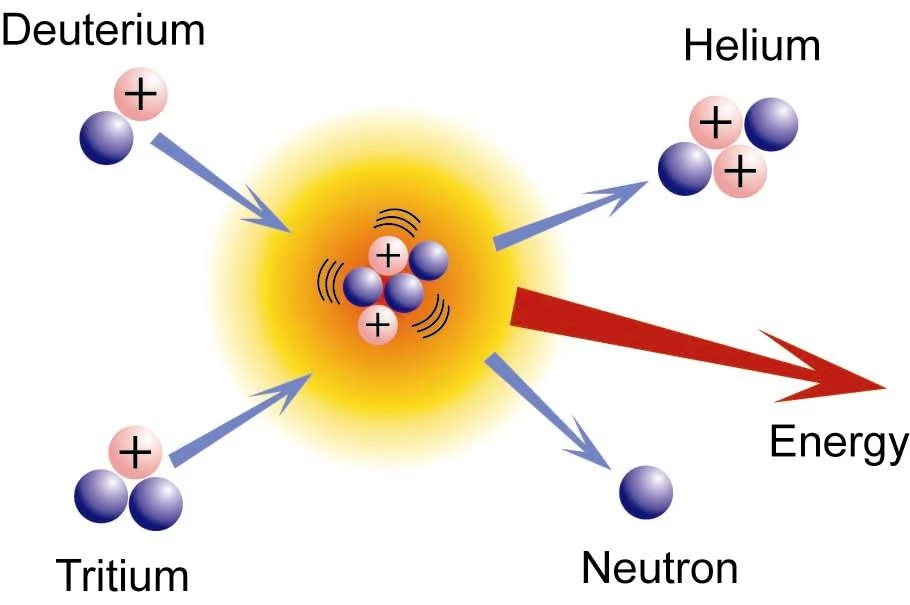
Будова атомів в молекулах призводить до зміни фізичних властивостей води. Нижче ви можете порівняти показники для різних вод.
|
Параметр |
D2O |
HDO |
H2O |
|
Температура плавлення, °C |
3,82 |
2,04 |
0,00 |
|
Температура кипіння, °C |
101,4 |
100,7 |
100,0 |
|
Густина при 20 °C, г/см³ |
1,1056 |
1,054 |
0,9982 |
|
pH при 25 °C |
7,41 |
7,266 |
7,00 |
Варто розуміти, що важка вода в природі існувала завжди, та її кількість не збільшилася і не зменшилася. Цікаво, що в гірських джерелах її менше, ніж в інших поверхневих водоймах.
Радіоактивність важкої води
Варто відзначити, що дейтерій і кисень O16, O17, O18 не є радіоактивними ізотопами, як, відповідно, і їх сполуки.
Щодо тритію, період його напіврозпаду дорівнює 12 рокам. Він дійсно має високу радіотоксичність, як і ряд атомів кисню. При цьому важливо розуміти що вміст тритію в воді менший, ніж 1:1018 мільйонів атомів водню. Його просто неможливо виявити в природних водах.
Причиною його надходження в навколишнє середовище є безперервні ядерні реакції, що відбуваються в атмосфері. Звідси можна прийти до висновку, що він також існує в воді мільйони років і не може впливати на здоров'я людини.
Найбільше тритію в дощі та снігу, найменше в океанічній воді. А в глибинних льодах Антарктиди його просто немає, оскільки він повністю розпадається.
Отримання важкої води
До 1946 року важка вода утворювалась лише завдяки електролізу, пізніше з'явилися технології ректифікації рідкого водню, а також ізотопного обміну в різних системах (водень/аміак, водень/вода, сірководень/вода).
У сучасному виробництві використовують метод, в якому вихідною (початковою) водою є стоки електролітичних цехів отримання водню. Вона містить до 0,2% важкої води. Після застосовується технологія ізотопного обміну в системах сірководень/вода, де відбувається концентрування до 5 - 10%. І на кінцевому етапі проводиться ступінчастий електроліз лужного розчину з отриманням ступеню чистоти дейтерієвої води 99,75 - 99,995%.
Вартість дейтерієвої води відрізняється в залежності від її чистоти. Для прикладу, грам води з вмістом атомів дейтерію від 70% загального числа водню коштує приблизно 0,8 $, а грам води містить вже понад 99,6% коштує 2,5 $.
Якщо розглянути отримання важкої води вдома з точки зору технології виробництва, яка описана вище, ви здогадаєтеся, що це неможливо. Існує теорія, що її можна отримати частковим заморожуванням води, за рахунок різниці температур замерзання води. Теоретично даний метод може допомогти вам підвищити вміст дейтерію на 10-20%, але доцільність цих маніпуляцій залишається під великим питанням. Така вода не має практичного застосування.
Використання

Існує кілька сфер застосування важкої води.
- Енергетика. Існують ядерні реактори, в яких важка вода застосовується в якості теплоносія. Її використання дозволяє використовувати природний уран більш низького ступеня збагачення.
- У лабораторіях. Як індикатор і розчинник в фізико-хімічному аналізі, в дослідженнях біологічних об'єктів, а також живих організмів, в тому числі людини.
- В медицині. Крім лабораторних досліджень людини, важка вода може застосовуватися для лікування грибків і бактерій, гіпертензії та ін.
Вплив на людину
Вище ми акцентували на головному факторі - чи шкідлива важка вода? Оскільки її вміст стабільний в атмосфері вже протягом багатьох тисячоліть, то її невисокі кількості у питній воді точно не є небезпечними для людства.
Що стосується експериментів із застосуванням концентрованої дейтерієвої води, то її не дарма називають мертвою водою.
Через відмінності фізичних властивостей, зокрема, густини, вона складніше проходить через клітинні мембрани, тому фактично пригнічує життєдіяльність. А через більш міцні водневі зв'язки хімічні реакції уповільнені.
Найпростіші можуть адаптуватися до 70-% води, а водорості здатні жити й розмножуватися навіть у 99% дейтерієвій воді.
Що стосується ссавців, тут заміщення 25% відсотків води призводить до неможливості давати потомство. Також великий обсяг важкої води мав ефективність при лікуванні ракових пухлин, але при цьому приводив до смерті тварини.
Людина може спокійно випити кілька склянок важкої води без будь-якого впливу на стан внутрішніх органів і самопочуття. Сьогодні така вода використовується для лікування певних випадків гіпертонії, що доводить відсутність побічних ефектів навіть при регулярному застосуванні її невеликих кількостей.
Варто також відзначити, що в організмі людини міститься певна кількість важкої води - рівна тій, що знаходиться в п'яти грамах звичайної води.
Важка чи жорстка вода?

Коли ми вивчали публікації про важку воду в інтернеті, дізналися, що деякі люди плутають її з "твердою" чи "жорсткою".
Тверда вода — це вода, яка містить певну кількість солей твердості, переважно карбонатів кальцію і магнію. Тверда — вода це про вапняний наліт і накип.
Що таке легка вода
Легкою є вода, яка містить меншу концентрацію дейтерієвої води. Хтось намагається виготовити її вдома, а хтось купує. Як ми писали вище, важка вода є природним компонентом поверхневих і питних вод, які вживали наші предки. Яких-небудь підтверджених клінічних досліджень про терапевтичний ефект такої води не існує.
Чи можна очистити воду від дейтерію вдома?
Ніякі фільтри для води, зокрема системи зворотного осмосу не здатні затримувати дейтерієву воду, оскільки між частинками дейтерію і протію немає істотних відмінностей.
Ми вже писали в нашому блозі про очищення води заморожуванням. Теоретично цей метод здатний видалити певну кількість важкої води, але раціональність цих маніпуляцій залишається під питанням.
У цьому тексті ми спробували пояснити, що являє собою важка вода, де її шукати, і як з нею жити. Також сподіваємося, що вдалось розвіяти популярні псевдонаукові міфи та занепокоєння наших клієнтів та читачів.
Якщо у вас залишилися питання, пишіть в коментарях. З радістю дамо відповідь.
 (050) 384-17-65
(050) 384-17-65