Що таке кислотний дощ?

Дощову воду чомусь часто називають ідеалом чистоти. Насправді, якщо дивитися на неї з хімічної точки зору, складно погодитися з подібним. Сьогодні ми розкажемо про кислотний дощ, і звідки, він береться.
Ok google. Чому йде дощ?
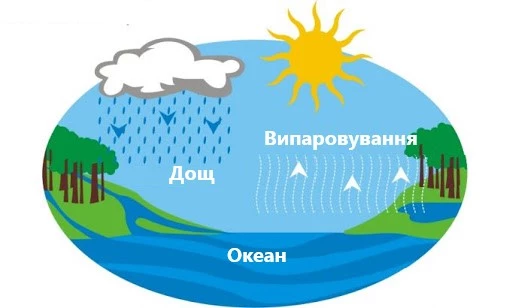
Щоб розуміти, як кислота потрапляє в дощову воду, варто розібратись, яким чином формується дощ. Існує колообіг води в природі. Коли сонце світить на поверхню води, що знаходиться в океанах і поверхневих водоймах, вона починає випаровуватися. Ми можемо спостерігати подібний процес при кипінні води, коли над нею виділяється пара. На водній поверхні в природних процесах її побачити складно, проте молекули води відриваються від водної гладі та злітають в повітря. Про унікальну властивість води перебувати в трьох агрегатних станах і процесах випаровування ми писали раніше .
Ці молекули підіймаються з повітряними масами все вище і вище, проходячи через шари холодного повітря, вони охолоджуються і конденсуються (об'єднуються) в краплі та дрібні крижані кристали в залежності від висоти. Скупчення переохолоджених крапель води та крижаних кристалів називаються хмарою.
Коли маса кристалів стає критичною, вона випадає на землю дощем.
Чому виникає кислотний дощ?
Дощова вода в хмарах є практично дистилятом, оскільки отримується в результаті випаровування. Її хімічні зміни починають відбуватися вже в момент падіння крапель на землю і проходження атмосфери, тобто оточуюючого нас повітря. Відповідно, водневий показник, який описує кислотність, дорівнює приблизно 7.
Почнемо з того, що спочатку повітря, яким ми дихаємо, містить від 0,9% вуглекислого газу. Розчинність вуглекислого газу у 28 разів перевищує кисень. Тобто в процесі руху крапля води насичується вуглекислотою, внаслідок чого утворюється слабка вуглекислота:
CO2 + H2O ⇄ CO2 + H2O.
Водневий показник, тобто pH чистого дощу в момент удару об землю може становити 5,6. Оскільки вугільна кислота є досить слабкою, вона швидко розкладається і виділяється з води.
Але в сучасному світі все складніше, крім вуглекислого газу повітря багате величезною кількістю інших сполук. У великих містах та індустріальних центрах забруднення повітря отримало назву "смог".
У питанні кислотного дощу варто згадати оксиди сірки й азоту. Ці речовини потрапляють в повітря як продукти спалювання органічного палива на теплоелектростанціях, в автомобілях, виробничих процесів металопереробних заводів та інших підприємств. Вони здатні викликати сухість слизових очей і носа, кашель, загострення легеневих захворювань.

Діоксид азоту (NO2) - це найпоширеніший компонент смогу. При недосконалому очищенні, він виділяється при згорянні палива на теплоелектростанціях і навіть з вихлопних труб автомобілів. Має характерний рудий колір, за що отримав назву "лисячий хвіст".
Монооксид азоту (NO) - при згорянні виділяється разом з діоксидом і утворює димери (N2O2).
Діоксид сірки (SO2) - це прозорий газ, який у великих концентраціях є токсичним, в слабких - вражає слизові оболонки очей і носоглотки.
Сірчаний ангідрид або триоксид сірки (SO3) виділяється переважно на хімічних підприємствах.

Механізм реакції цих газів з водою дуже простий.
1. При взаємодії з водою і киснем повітря діоксид азоту утворює азотну кислоту:4NO2 + 2H2O + O2 ➝ 4HNO3
2. Паралельно відбувається окиснення діоксиду сірки діоксидом азоту з отриманням сульфатної кислоти:NO2 + SO2 + H2O ➝ H2SO4 + NO
3. І ще один процес являє собою утворення сірчаної кислоти з ангідриду:SO3 + H2O ➝ H2SO4
Ось так, власне, і виглядає відповідь на питання про те, що таке кислотні дощі.
Кислотність, якщо використовувати для її зображення рівня pH середовища, може досягати 3 одиниць. Для порівняння pH слабкого розчину лимонної кислоти буде приблизно таким же. Опади з pH <5,6 називають кислими, вони можуть викликати зрушення кислотно-лужної рівноваги в ґрунтах і водоймах, спричиняти видові зміни або вимирання флори та фауни.
Важливо відзначити, що іноді дощова навіть в промислових регіонах або великих містах має нейтральний або навіть легколужний pH. Це не говорить про якість або чистоту, а лише про те, що через реакції всередині крапель кислота нейтралізувалася лужними реагентами. Найяскравішим прикладом буде наявність аміаку в повітрі:
NH3 + HNO3 ⟶ NH4NO3
Хімічні процеси безперервно відбуваються навіть у краплі води, поки вона летить з неба на землю.
Як бачите, забруднення навколишнього середовища робить небезпечним навіть найчистішу дощову воду.
 (050) 384-17-65
(050) 384-17-65